RESEARCH
生命とは? その追及が人類を進化させる
ミッション
生命とは何か。「自己複製」と「進化」にその答えがあると思っています。
複製する中で変異による多様性が生じ、環境に応じて優位に複製するものが淘汰され、次の世代に情報が継承されます。
このサイクルを生命は40億年かけて続け、現在の地球上での繁栄に至ったわけです。既存の分子生物学は、このような複雑かつ多様に進化した個々の生命現象
を分子レベルで記述するのに力を発揮してきました。一方でそもそも、どのようにして複雑に進化する能力を備えた分子システムが誕生したのでしょうか。そのようなシステムを人工的につくりだすことはできるのでしょうか。
研究室では、 複製装置や転写翻訳装置などを試験管内で組み合わせていくボトムアップアプローチと、 ゲノムを合成して生きた細菌に移植するトップダウンアプローチにより、 「自己複製して進化するウェットな生化学システムをつくる」ことを目指します。 生命は進化することで危機的な局面を乗り越えてきました。自己複製と進化をエンジニアリングして活用できれば、 「バイオテクノロジーによる地球規模の課題解決」にもつながると考えます。
研究室では、 複製装置や転写翻訳装置などを試験管内で組み合わせていくボトムアップアプローチと、 ゲノムを合成して生きた細菌に移植するトップダウンアプローチにより、 「自己複製して進化するウェットな生化学システムをつくる」ことを目指します。 生命は進化することで危機的な局面を乗り越えてきました。自己複製と進化をエンジニアリングして活用できれば、 「バイオテクノロジーによる地球規模の課題解決」にもつながると考えます。
*ボトムアップでつくる細胞を「人工細胞」、トップダウンでつくる細胞を「合成細胞」と呼んでいます
アプローチ
研究室の強み
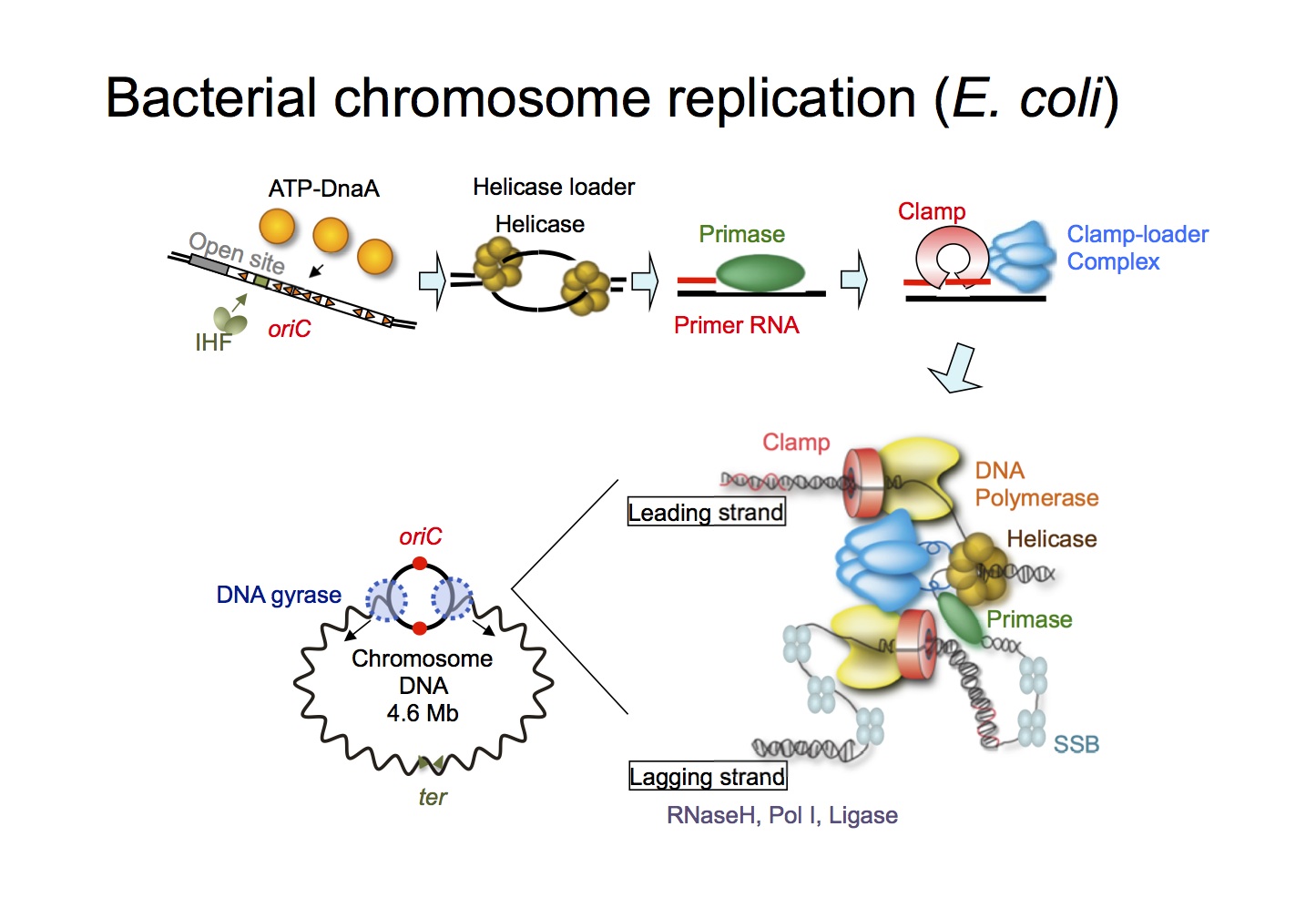
自己複製の最初のステップは、生命の設計図であるゲノムの複製です。 研究室の強みは、ゲノム複製の完全なサイクルを精製タンパク質を組み合わせることで人工的に再現することに成功したことです(Su'etsugu et al., 2017 NAR)。 とても苦労しましたが、おかげで今のところ、この複製サイクル再構成系(RCR)を作れるラボは世界でもウチだけです。
ボトムアップアプローチ
すでに転写翻訳の試験管内再構成系は完成されているので、複製サイクル再構成系と合わせて、セントラルドグマ(複製・転写・翻訳)の全工程を試験管内で回すことができそうです。 それにより達成されるのが自己複製であり、また複製エラーを通じたゲノムの進化です。
トップダウンアプローチ
再構成系における複製サイクルの自律的な繰り返しは、新しいDNA増幅技術としても画期的です。 化学合成された短いDNAをたくさん繋ぎ合わせてゲノムを合成しますが、細胞を使わずにゲノムサイズの長いDNAを増やす技術がありませんでした。 複製サイクル再構成系は100万塩基対ものとても長い環状DNAを増幅できる唯一の反応系です(Mukai et al., 2020 ACS Synth. Biol.)。 細胞の制約なしにデザインされたゲノムを合成できるようになると考えています。
そして、合成ゲノムを細胞に移植して起動できれば合成細胞も期待されます。 ゲノムサイズの長いDNAを細胞に移植する技術は長年課題でしたが、我々は大腸菌に100万塩基対の長いDNAを移植することにも世界で初めて成功しました(Yoneji et al., 2021 NAR)。
情報としてのゲノム
生命情報であるゲノムを計算機上でデザインし、人工/合成細胞を作製して検証する研究は、自動化やIT・AI分野の進展も相まって今後の生命科学の新しい潮流になりつつあります。
また、ゲノム(DNA)はA/G/C/Tの4つの文字で情報を高密度にコードできるという特徴から、半導体に変わる新しい情報記憶媒体(DNAストレージ) としても注目されます。 ここでも我々の技術が活用できると思っています。
半導体時代の次にくる次世代ナノテクノロジーとしてのDNAとセントラルドグマに着目しています。
自己複製の最初のステップは、生命の設計図であるゲノムの複製です。 研究室の強みは、ゲノム複製の完全なサイクルを精製タンパク質を組み合わせることで人工的に再現することに成功したことです(Su'etsugu et al., 2017 NAR)。 とても苦労しましたが、おかげで今のところ、この複製サイクル再構成系(RCR)を作れるラボは世界でもウチだけです。
ボトムアップアプローチ
すでに転写翻訳の試験管内再構成系は完成されているので、複製サイクル再構成系と合わせて、セントラルドグマ(複製・転写・翻訳)の全工程を試験管内で回すことができそうです。 それにより達成されるのが自己複製であり、また複製エラーを通じたゲノムの進化です。
トップダウンアプローチ
再構成系における複製サイクルの自律的な繰り返しは、新しいDNA増幅技術としても画期的です。 化学合成された短いDNAをたくさん繋ぎ合わせてゲノムを合成しますが、細胞を使わずにゲノムサイズの長いDNAを増やす技術がありませんでした。 複製サイクル再構成系は100万塩基対ものとても長い環状DNAを増幅できる唯一の反応系です(Mukai et al., 2020 ACS Synth. Biol.)。 細胞の制約なしにデザインされたゲノムを合成できるようになると考えています。
そして、合成ゲノムを細胞に移植して起動できれば合成細胞も期待されます。 ゲノムサイズの長いDNAを細胞に移植する技術は長年課題でしたが、我々は大腸菌に100万塩基対の長いDNAを移植することにも世界で初めて成功しました(Yoneji et al., 2021 NAR)。
情報としてのゲノム
生命情報であるゲノムを計算機上でデザインし、人工/合成細胞を作製して検証する研究は、自動化やIT・AI分野の進展も相まって今後の生命科学の新しい潮流になりつつあります。
また、ゲノム(DNA)はA/G/C/Tの4つの文字で情報を高密度にコードできるという特徴から、半導体に変わる新しい情報記憶媒体(DNAストレージ) としても注目されます。 ここでも我々の技術が活用できると思っています。
半導体時代の次にくる次世代ナノテクノロジーとしてのDNAとセントラルドグマに着目しています。
テクノロジーのスピンオフ
基礎研究の成果を新しいテクノロジーとしてスピンオフします。染色体複製サイクルの繰り返しを20種以上の酵素を用いて試験管内再構成した反応系
(RCR; Su'etsugu et al., 2017
NAR)は、複製サイクル全反応の必要十分条件を明らかにしただけでなく、ゲノムスケールの長鎖DNAをセルフリーで増幅可能とする新技術を生み出しまし
た。誰でもこの技術が使えるよう、キット化しています(バイオセキュリティーの観点を考慮し、使用に当たっては同意書の提出を求めています)。なおOriCiro Genomics社からの一般販売は終了となりました。
※バイオセーフティー、バイオセキュリティー(デュアルユース)について
・複製サイクル再構成系(RCR)はデザインされたゲノムスケールの長鎖DNAを合成して、有用な改変細胞等を生み出すことにつながる技術です。 一方で、想像されるその倫理的な問題やリスクについて、十分配慮して研究を進める必要があります。
・病原性や感染性の生物(ウイルス)のゲノムを、"細胞を使わずに試験管内で"増幅させる実験については、 いまのところ法令やガイドラインの定めはありませんが、十分注意管理して進める必要があります。 (増幅したDNAを細胞に入れる場合は、当然カルタヘナ法の対象となります)
合成生物学のELSI(Ethical, Legal and Social Issues)
合成生物学は従来の遺伝子組み換え技術の延長と捉えることもできますが、技術的には合成細胞を作製できるレベルになっています。 2010年にベンター研究所が合成細菌を発表した際には、大統領諮問委員会にて合成生物学のリスク検証がなされ、 「現段階ではリスクは限定的であり、慎重な自己規制のもとで発展させることで、様々な分野を革新する可能性がある」とされました。 ただし技術進展により、将来新たな課題が生まれる可能性はあり、継続した議論が大事です。 例えば、DNA合成技術の進展は、上述のようなデュアルユースの懸念をはらんでおり、 一方で、新興感染症に対するmRNAワクチン開発に貢献し人々を救っています。 この分野は特に、一般社会の漠然とした恐怖を煽りやすいこともあり、正しい発展のためにも、 研究者自身がそのメリットとリスクを正確に情報発信し対話していくことが求められると思います。参考: JST RISTEX ゲノム倫理研究会 ケーススタディ 「末次プロジェクト」
(2023年に半年間、各種専門家や市民などと、末次の研究およびゲノム合成のELSIについて議論を交わしました。報告書はこちら)
長鎖DNA設計ツール
人工ゲノム合成技術(開発中)におけるDNA断片設計のために作ったシンンプルなオンラインツール。
(by Ryo Hirata, Su'etsugu lab B4, 2016)
バナースペース
末次研究室
立教大学理学部
〒171-8501
東京都豊島区西池袋3-34-1